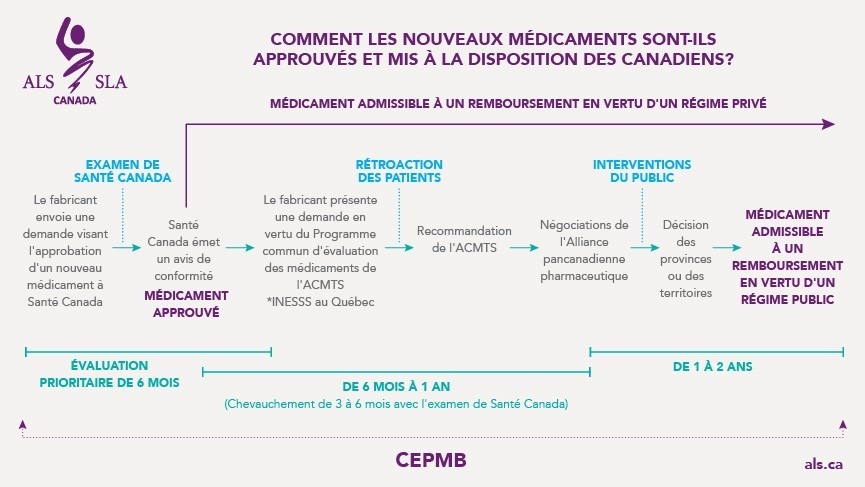
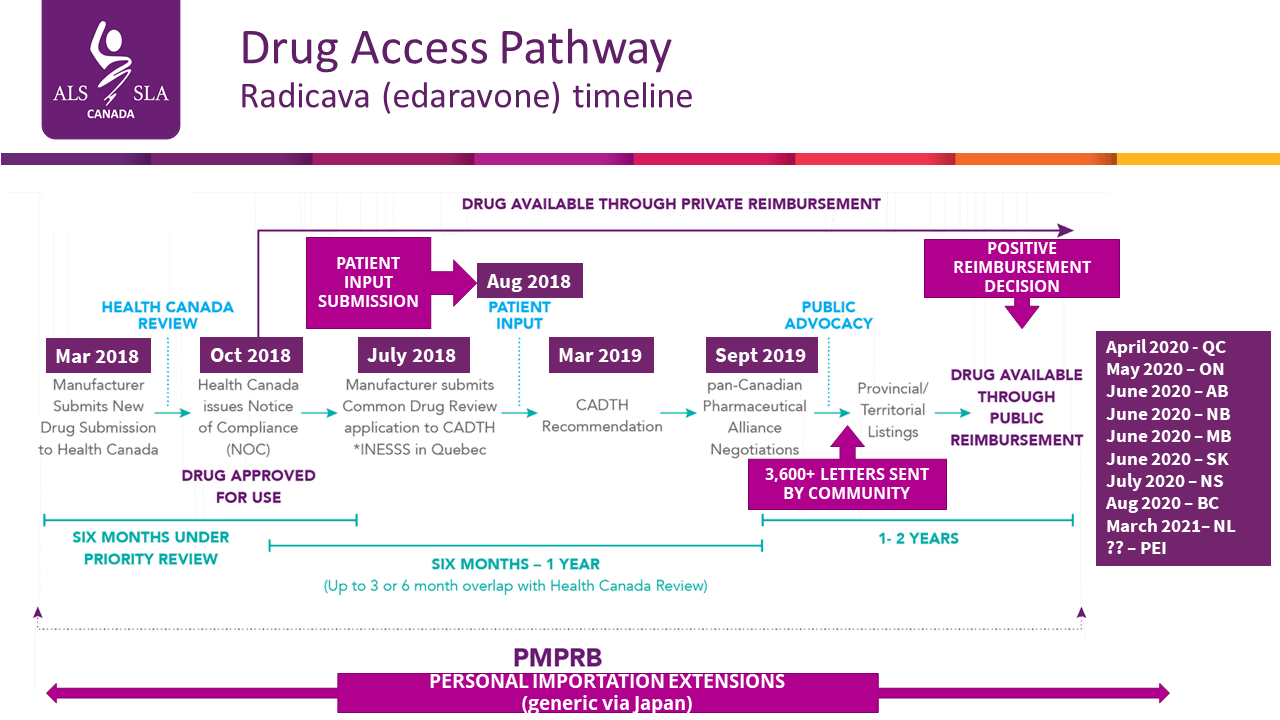
Fonctionnement
Le fabricant du médicament présente une demande au titre du Programme commun d’évaluation des médicaments, qui est régi par un organisme fédéral appelé Agence canadienne des médicaments et des technologies de la santé (ACMTS). (Au Québec, ce processus est géré par l’Institut national d’excellence en santé et en services sociaux [INESSS].)
Le Programme commun d’évaluation des médicaments évalue les preuves cliniques et économiques du médicament, et celles relatives aux patients et aux cliniciens. Il en résulte des recommandations et des conseils qui sont utilisés par les régimes fédéraux, provinciaux et territoriaux d’assurance-médicaments pour décider si les coûts du médicament seront couverts par des programmes publics.
La rétroaction des patients et, depuis 2020, celle des cliniciens, sont des éléments clés du Programme commun d’évaluation des médicaments. Les groupes de patients sont invités à partager leurs expériences, perspectives et attentes à l’égard du médicament évalué, alors que les cliniciens ont l’occasion de formuler des commentaires sur les avantages du traitement d’un point de vue clinique. Ensemble, les patients et les cliniciens renseignent l’ACMTS sur les réalités d’un diagnostic de SLA et sur la façon dont les traitements qui ont un impact, si modeste qu’il soit, peuvent sensiblement améliorer la qualité de vie des patients.
La Société canadienne de la SLA prévoit recueillir la rétroaction des patients au sujet d’AMX0035 à l’intention de l’ACMTS et invitera la communauté canadienne de la SLA à contribuer à cette démarche. Si vous désirez y participer, abonnez-vous à notre bulletin électronique pour être avisé.
À la fin du Programme commun d’évaluation des médicaments, on émettra l’une des recommandations suivantes :
- que le médicament soit remboursé;
- que le médicament soit remboursé selon des critères ou des conditions cliniques; ou
- que le médicament ne soit pas remboursé.
La recommandation finale est transmise aux régimes d’assurance-médicaments participants et au fabricant, puis affichée sur cadth.ca.
Après l’achèvement du Programme commun d’évaluation des médicaments, les régimes d’assurance-médicaments du fédéral, des provinces et des territoires peuvent choisir de collaborer par l’intermédiaire de l’Alliance pancanadienne pharmaceutique (APP) afin de déterminer le fonctionnement d’un remboursement public dans chaque territoire de compétence en fonction de négociations effectuées avec le fabricant.
Ensuite, chaque territoire de compétence réalise généralement son propre examen indépendant pour déterminer si le médicament sera couvert par les régimes publics d’assurance-médicaments, et de quelle façon. Une fois l’examen terminé, les autorités sanitaires du territoire de compétence (p. ex., le ministère de la Santé) prendront la décision définitive concernant la couverture en vertu du régime public d’assurance-médicaments. Les régimes d’assurance-médicaments publics qui décident de couvrir le traitement, en totalité ou en partie, concluent une Entente de remboursement avec le fabricant.
De plus en plus, les régimes d’assurance-maladie privés font référence à la recommandation de l’ACMTS au moment de décider s’ils couvriront ou non un médicament.
Combien de temps dure le processus?
- En 2018, Santé Canada, l’ACMTS et INESSS ont annoncé le lancement d’un programme d’examen coordonné, en vertu duquel le Programme commun d’examen des médicaments acceptera des soumissions six mois avant la réception prévue d’un avis de conformité de la part de Santé Canada.
- Le délai cible du Programme commun d’évaluation des médicaments est d’environ six mois. Cependant, il existe plusieurs variables qui peuvent influer sur le processus et le prolonger d’une année ou plus.
- Les échéanciers relatifs aux travaux de l’Alliance pancanadienne pharmaceutique et, subséquemment, aux Ententes de remboursement avec les régimes d’assurance-médicaments peuvent s’échelonner sur jusqu’à deux ans, selon le territoire de compétence. Cependant, il existe souvent, tout au long du processus, des moyens pour les patients, les groupes de patients et les aidants de faire pression pour accélérer le processus.